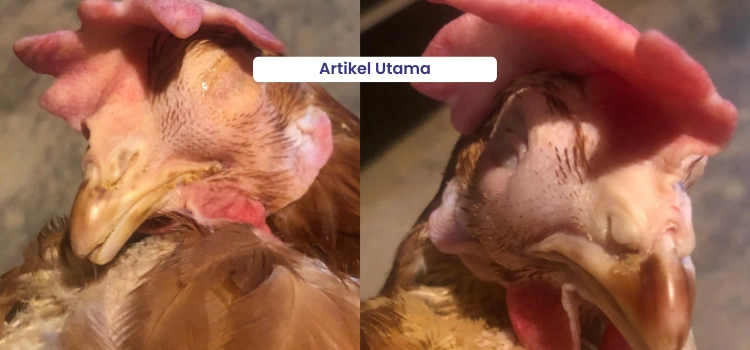
Worms are a parasitic disease in chickens that require attention in the poultry industry because they significantly impact livestock health, welfare, and productivity. Direct losses from worms include decreased FCR (Feed Conversion Ratio), livestock weight gain, egg production, egg quality, and mortality in cases of chronic infection. Indirect losses include damage to the intestinal mucosa due to worm infestation in the digestive tract and immunosuppressive effects, which increase susceptibility to other infections.

Based on findings of clinical symptoms and anatomical pathology changes carried out by the Medion field personnel team, in the last three years before the production period of layer chickens, the percentage of worm cases in 2023, 2024, and 2025 respectively reached 2.04%, 2.66%, and 1.86%, while the percentage of cases during the production period of layer chickens in the 3 years respectively reached 13.35%, 13.12%, and 12.76%. The higher number of worm cases during the production period of layer chickens is related to the worms' long life cycle and the possibility of repeated exposure during that phase.
Factors that directly influence the incidence of parasitic infections in chickens include the host, parasite, and environment. Host factors include chicken species, age, and sex. Parasite factors that influence the parasite include transmission mode, parasite survival in the environment, pathogenicity, and immunogenicity. Environmental factors that influence the parasite include weather, temperature, humidity, cage management, vectors or intermediate hosts, and the use of anthelmintic drugs.
High rainfall, coupled with fluctuating temperatures and high humidity, creates a favorable environment for worm eggs to develop into the infective phase. Moist conditions are also favorable for worm vectors such as beetles, flies, slugs, and snails.
Worm infections are more common in poultry raised in open houses and semi-closed houses than in closed houses. Furthermore, the postal rearing system also makes poultry more susceptible to worm infections compared to battery cages. This system places poultry in direct contact with feces and bedding containing infective stages of worm eggs. Poultry raised in open or semi-closed houses are also more susceptible to worm infections because environmental control, particularly against worm vectors, is more difficult than in closed cages.


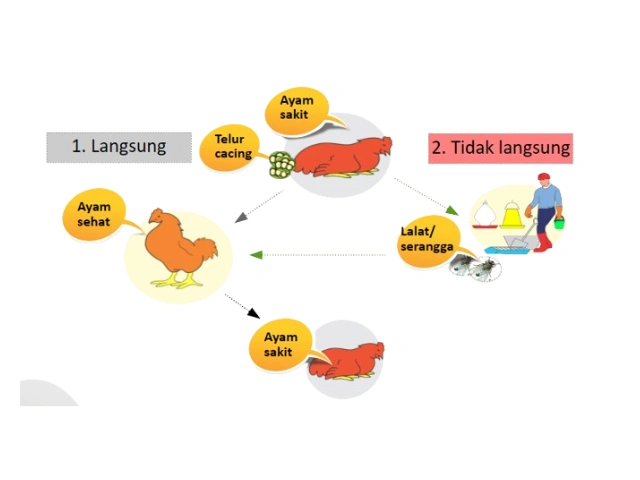
The livestock husbandry system is a crucial factor to consider because worm transmission can occur horizontally, either directly from sick chickens to healthy chickens, or indirectly through environmental contamination, equipment and personnel, and vectors. Worm eggs found in the feces of infested chickens can contaminate litter, cage equipment, and the surrounding environment. In such cases, healthy chickens that accidentally ingest the eggs become infected. This cycle will repeat itself if control measures are not taken.
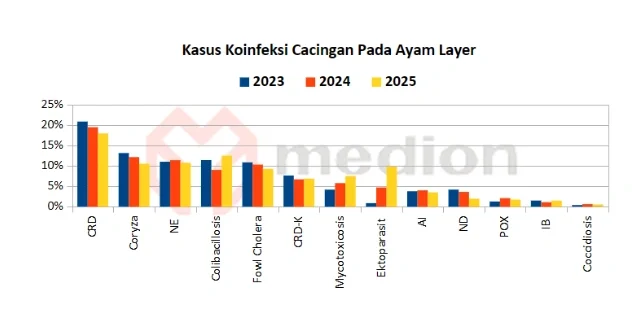
In laying hens, losses due to worms not only cause a 5-20% decrease in egg production but also lead to immunosuppression, making them susceptible to other infections. Based on data collected by Medion's field team, cases of worms in laying hens are always accompanied by other infections, including bacterial, viral, fungal, or parasitic infections. Over the past three years, field case findings have shown that laying hens diagnosed with worms based on clinical symptoms and anatomical pathological changes also exhibit co-infections such as CRD, Coryza, Colibacillosis, NE, Fowl Cholera, Coccidiosis, Ectoparasites, AI, ND, POX, IB, and Mycotoxicosis.
In general, poultry can be infected with various types of worms, such as roundworms (nematodes), tapeworms (cestodes), flatworms (trematodes), and Acanthocephala. However, the most common worm infections found in the field are roundworms (nematodes), tapeworms (cestodes), and Acanthocephala.

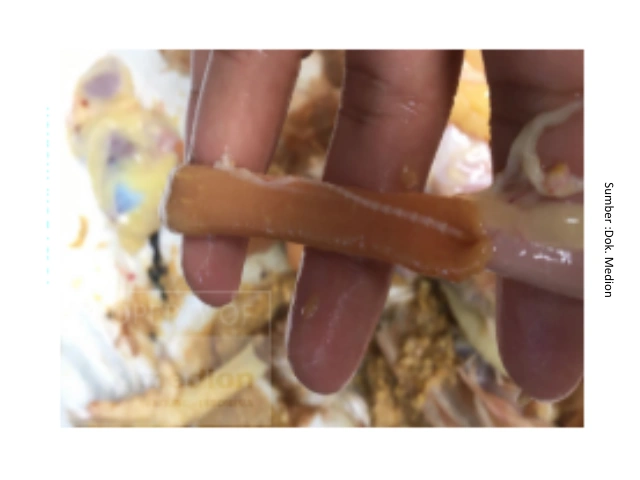
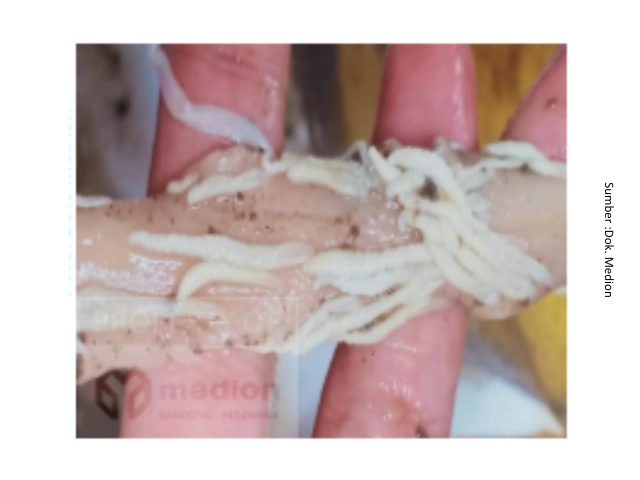
The findings of these cases were also explained by Abd El-Ghany (2022), who stated that worm infections in the digestive tract of poultry, especially those caused by roundworms, are the most common group of parasites infecting poultry both in terms of the number of species and the severity of the infection. Some common families found include Heterakidae, Capillaridae, Syngamidae, and Trichostrongylidae. In addition to roundworms, tapeworms are also commonly found in poultry with varying levels of pathogenicity, ranging from mild to severe. Tapeworms that infect poultry generally come from three main families: Davaineidae, Dilepididae, and Hymenolepididae, with several frequently reported genera such as Raillietina, Davainea, and Hymenolepis. Meanwhile, flatworms/leafworms have lower host specificity than roundworms and tapeworms in farmed poultry. Cases of Acantocephala have also been found frequently in the field. Initial reports of these cases in Indonesia occurred in Yogyakarta and several areas in Central Java such as Magelang, Klaten, and Solo. In recent years, Medion's field personnel team has also discovered Acantocephala worm infections in East Java, namely Blitar and Mojokerto.
Roundworms (Nematodes)
Roundworms (nematodes) are a type of worm with a round, elongated body shape and no proglottids (body segments). Adult worms generally range in size from 6–13 cm, with a primary location of preference in the digestive tract, particularly the small intestine and cecum. Some species of roundworm that frequently infect poultry include Heterakis gallinarum, Capillaria sp., Ascaridia galli, Oxyspirura sp., Syngamus trachea, and Trichostrongylus sp., each of which can cause health problems of varying severity.
The life cycle of roundworms in poultry is generally direct, requiring no vector or intermediate host. Transmission occurs through the consumption of feed, drinking water, litter, or other materials contaminated with feces containing infective eggs. Worm eggs excreted in the feces develop in the environment and become infective within approximately 14 days. When these infective eggs are ingested by chickens, the larvae develop inside the body and become adult worms in approximately 45 days, making re-infection possible if cage sanitation is not maintained properly.
Tapeworms (Cestoda)
Tapeworms (cestodes) are flat worms with proglottids (body segments), with an adult body length of about 25 cm. These worms generally live in the small intestine and are hermaphrodite (having two sexes in one body, male and female), and have suckers and hooks used to attach to the intestinal wall of their host. Some species that often infect poultry include Raillietina sp., Davainea sp., Hymenolepis sp., and Moniezia sp. Unlike roundworms, the life cycle of tapeworms requires a vector/intermediate host. Worm eggs that are excreted in feces will develop in about 5 days, then be ingested by an intermediate host such as an insect, and then develop into an infective form in about 12–18 days before finally being able to infect poultry when the intermediate host is swallowed.
Acanthocephala worms
Acanthocephala worms are a group of worms with their own phylum and are distinct from other types of worms that commonly infect poultry. According to literature presented by McMullin (2020) and Otranto (2024), this group is closely related to roundworms. Acanthocephala worms are known as "thorny-headed worms" because they have a distinctive proboscis structure, a kind of trunk or protrusion on the head (anterior) equipped with small spines for attaching to the intestinal wall of their host. Acanthocephala worms have a complex life cycle with the help of a vector/intermediate host, namely an arthropod.
Worm eggs ingested by the intermediate host hatch, and the larvae (called acanthors) migrate into the arthropod's body and develop into the infective form (called cystacanths) in about 1–3 months. Chickens, or definitive hosts, become infected when they eat the arthropods. After entering the digestive tract, they attach to the intestinal wall and develop into adult worms. The time from infection to the worms' egg production ranges from 5 to 12 weeks.
Pathogenesis of Worms and Their Impact on Poultry Performance
In general, worm infections in chickens, particularly those that infect the digestive tract, significantly impact performance and health due to damage to the digestive tract mucosa and immunosuppressive effects. Infective worm eggs ingested by chickens develop in the digestive tract, eventually developing into adult worms. Worms that develop in the chicken's intestines absorb nutrients consumed by damaging the intestinal mucosa and the local immune system as they attach to the lumen of the intestinal wall. This condition can lead to damage and ultimately dysfunction of the intestines, preventing them from digesting food. Furthermore, the chickens experience discomfort due to the worms' activity along their digestive tract.
Roundworm species, such as Ascaridia galli, which have a life cycle without a vector/intermediate host, not only damage the intestinal mucosa of chickens but also make it a breeding ground for larvae, thus increasing the impact. Nutrients from food, which should be utilized by chickens for growth and production, cannot be optimally absorbed due to the worms manifesting in the intestines. The resulting mucosal damage also leads to decreased intestinal function, such as fluid absorption and the local immune system in the digestive tract, resulting in diarrhea and immunosuppression in infected livestock.
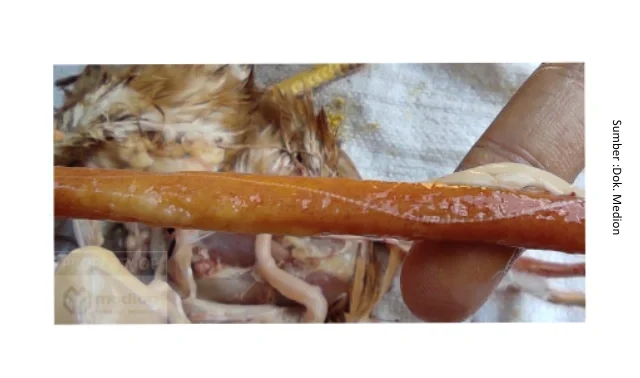
Worm Control in Laying Hens
Worms in poultry can be controlled through prevention and treatment. Prevention can be achieved through the following steps:
1. Regular administration of deworming medication
Preventive deworming of chickens can begin at 4 weeks of age and is administered periodically. Depending on the type of worm, repeat administration of medication for roundworm prevention can be done every 1–2 months, while for tapeworms, it is done every 1 month. This recommendation is based on the life cycle of each worm species. Based on the housing system, repeat deworming is recommended for postal cages every 1 month, and for battery cages every 3 months. This is due to the high risk of contact between chickens and infectious agents in postal cages, so repeat administration is necessary more frequently. Deworming can be administered through feed or drinking water. One anthelmintic product produced by Medion that can be administered through drinking water is WormisolThis product is effective against common worm infections in poultry, such as roundworms, tapeworms, and Acanthocephala. It works by paralyzing the worms and damaging the outer layer of the adult worms' bodies in the intestines, so that the worms will come out with the feces in the form of body parts. Wormisol given through drinking water which must be consumed within 4 hours, with a dose of 1 mL/L drinking water or 0.2 mL/kg body weight.

2. Vector Control
Some types of worms are parasites that require a vector/intermediate host to complete their life cycle. Therefore, controlling worm infestations in chickens must also consider the presence of vectors, such as flies, beetles, slugs, and snails. Vector control, particularly for flies, can be achieved by using insecticides or anti-fly medications such as Larvastop, Larvarox, and Flytox, which is effective in controlling fly populations in the cage environment.
3. Management and Biosecurity
Implementing good husbandry management and biosecurity is a crucial step in controlling various diseases, including worm infestation. Regular fecal cleaning can help break the chain of worm transmission and reduce the population of vectors such as flies. Furthermore, keeping the enclosure free of standing water and weeds is crucial to prevent vector development. Regular sanitation and disinfection of enclosures, equipment, and personnel are essential. Litter management is also crucial, especially in postal enclosure systems, to maintain cleanliness and suppress the development of infectious agents.
4. Routine Monitoring of Worm Infections
Routine monitoring of worm infections is an important step in preventing and controlling worm disease in chickens. Monitoring can be conducted in a laboratory, including in a poultry farm. MediLab to detect the presence of worm eggs in feces. The examination method can be qualitative to identify the type of worm infecting the animal, or quantitative to determine the severity of the infection. Fresh feces are used as samples, particularly from chickens showing signs of worms. In practice, this examination is generally performed before administering deworming medication and after repeating treatment to evaluate the effectiveness of the therapy.
Treatment for worms in chickens can be performed by administering deworming medication to birds that have been diagnosed, either through fecal examination or post-mortem examination. After treatment, regular deworming is recommended to prevent reinfection. Furthermore, regular fecal examinations are necessary to monitor for infection, while maintaining vector control, husbandry management, and good biosecurity practices.
Worms in laying hens are generally not a fatal disease compared to viral or bacterial diseases. However, to optimize production performance and maintain livestock health, controlling worm infections remains a priority. This is primarily because the resulting immunosuppressive effects can weaken the chicken's immune system, increasing its susceptibility to other infections.
Written references:
Abd El-Ghany, W. A. (2022). An updated insight into the gastrointestinal helminthoses of poultry: A review. Annals of Parasitology, 68(4).
Belo, AM, Suratma, INA, & Oka, IBM (2023). Prevalence of gastrointestinal nematode worm infections in laying hens in Peninjoan Village, Tembuku District, Bangli Regency, Bali. Udayana Veterinary Bulletin, 15(1), 20-27.
Hambal, M., Efriyendi, R., Vanda, H., & Rusli, R. (2019). 34. Anatomical Pathology and Histopathological Changes of Ascaridia Galli in Layer Chicken. Jurnal Medika Veterinaria, 13(2), 239-247.
McMullin, P. F. (2020). Diseases of poultry 14th edition.John Wiley & Sons
Otranto, D., & Wall, R. (2024). Veterinary parasitology. John Wiley & Sons.
Sanchez-Godoy, F. D., Martinez-Guzmán, J. R. E., Hernandez-Castro, R., Martinez-Hernandez, F., Urquiza-Bravo, & Hernandez-Velasco, X. (2024). Acanthocephaliasis by Plagiorhynchus sp.(Acanthocephala: Plagiorhynchidae) associated with necrotic enteritis in quetzals (Pharomachrus mocinno) maintained in captivity. Parasitology International, 103, 102954.
Shifaw, A., Feyera, T., Walkden-Brown, S. W., Sharpe, B., Elliott, T., & Ruhnke, I. (2021). Global and regional prevalence of helminth infection in chickens over time: a systematic review and meta-analysis. Poultry Science, 100(5), 101082.